- 사노피, 항-CD3 항체 ‘티지엘드’로 질병 변형 피망 바카라 시대 개막
- 버텍스·젠티바이오·폴트렉, 세포·면역피망 바카라로 ‘인슐린’ 독립 도전
- 릴리·오츠카 등 유전자편집·면역관용 플랫폼 가세…차세대 경쟁 본격화
[더바이오 성재준 기자] 제1형 당뇨병(Type 1 Diabetes, T1D) 치료가 기존의 ‘인슐린’ 중심 관리에서 ‘질병 변형(Disease-Modifying)’ 접근으로 점차 확대되고 있다. 항체, 세포, 면역, 유전자 치료 등 다양한 방식의 신기술이 임상 단계에 진입하면서 중장기적으로 치료 전략의 변화가 예상된다.
국제당뇨병연맹(IDF)에 따르면 전 세계 당뇨병 환자는 약 5억8900만명에 이르며, 이 가운데 제1형 당뇨병 환자는 약 920만명으로 추산된다. 불과 3년 전까지만 해도 이들에게는 인슐린이 사실상 유일한 피망 바카라 수단이었다.
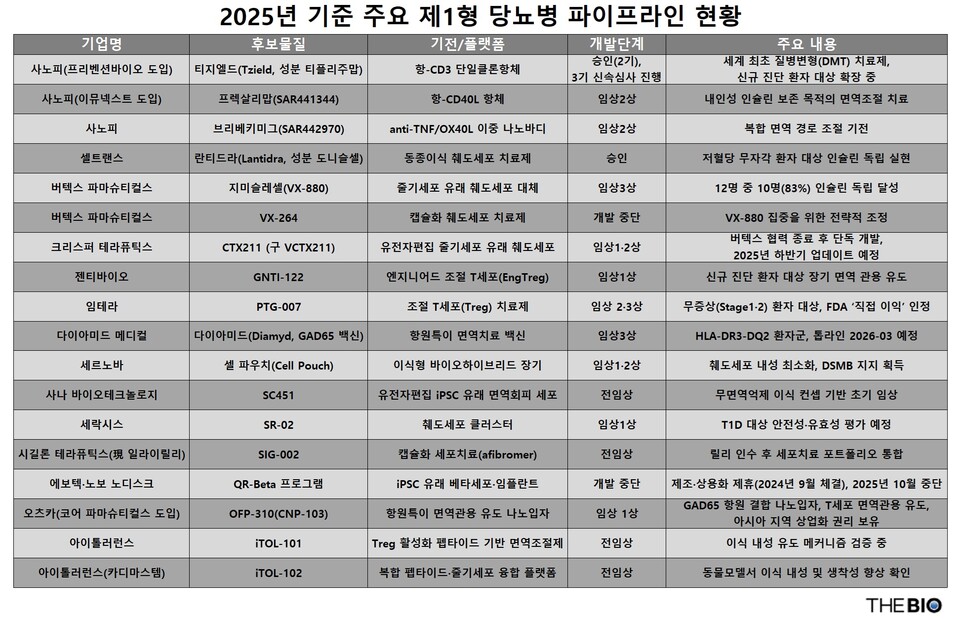
최근에는 인슐린 주사 중심의 기존 피망 바카라에서 벗어나, 면역 조절과 세포 대체를 기반으로 한 새로운 피망 바카라 접근법이 점차 구체화되고 있다. 3일 <더바이오가 집계한 결과 다국적 제약사 사노피를 비롯해 버텍스파마슈티컬스(이하 버텍스), 오츠카 등이 해당 피망 바카라제 개발 경쟁을 벌이고 있다.
◇사노피, 면역 조절 기반 질병 변형 피망 바카라로 T1D 공략
2022년 미국 식품의약국(FDA)이 다국적 제약사 사노피의 항-CD3 단일클론항체인 ‘티지엘드(Tzield, 성분 티플리주맙)’을 승인하면서 제1형 당뇨병 피망 바카라에 ‘질병 변형’ 개념이 처음으로 도입됐다. 이 약물은 현재 2기(발병 전 단계) 환자에서 사용되고 있으며, FDA는 지난 10월 신규 진단 3기(발병 초기) 환자군에 대한 ‘신속심사(expedited review)’를 개시해 적응증 확대가 유력한 상황이다.
사노피는 이와 별도로 ‘프렉살리맙(Frexalimab, 또는 개발코드명 SAR441344)’과 ‘브리베키미그(Brivekimig,또는 개발코드명 SAR441255)’ 등 2가지 면역 조절 후보물질을 임상2상 단계에서 개발하고 있다. 프렉살리맙은 항-CD40L 기전을, 브리베키미그는 ‘TNF’와 ‘OX40L’을 동시에 차단하는 이중작용 나노바디 기전을 기반으로 한다. 두 약물 모두 자가면역질환 전반으로 확장이 가능한 전략적인 파이프라인으로 평가되며, 사노피의 제1형 당뇨병 진입을 한층 가속화하고 있다.
◇세포·면역피망 바카라 확장…버텍스·젠티바이오·폴트렉 등 주도
세포피망 바카라 분야에서는 버텍스가 선두를 달리고 있다. 줄기세포 유래 췌도세포 피망 바카라제 후보물질인 ‘VX-880(ZVX-880, 성분 지미슬리셀)’은 임상1·2상에서 단회 투여 1년 후 12명 중 10명(83%)이 인슐린 독립을 달성해 주목받았다. VX-880은 현재 임상3상 단계에 진입했으며, 버텍스는 VX-264 프로그램을 종료하고 개발 역량을 VX-880에 집중하고 있다.
한편, 크리스퍼테라퓨틱스(CRISPR Therapeutics)의 ‘CTX211(개발코드명, 옛 VCTX211)’은 버텍스와의 협력 종료 이후 공동 개발이 중단됐지만 단독으로 임상이 진행 중이다. 주요 임상 데이터 업데이트는 올해 하반기에 예정돼 있다.
면역세포 기반 피망 바카라도 새로운 대안으로 주목받고 있다. 젠티바이오(GentiBio)의 ‘GNTI-122(개발코드명)’는 올해 7월 FDA로부터 임상시험계획(IND) 승인을 받았다. 이 후보물질은 ‘엔지니어드 조절 T세포(EngTreg)’를 이용해 내인성 인슐린을 보존하고, 장기적인 면역 관용 유도를 목표로 한다.
또 폴트렉(PolTREG)의 미국 자회사인 임테라(Immthera)는 무증상(1·2기) 환자를 대상으로 한 적응형 임상2·3상 단계 후보물질인 ‘PTG-007(개발코드명)’의 IND 제출을 준비 중이다. FDA는 해당 프로그램이 환자에게 ‘직접적인 임상 이익(direct benefit)’을 제공할 가능성이 있다고 평가했다.
◇차세대 플랫폼 확장…세포 이식·유전자 편집·면역 관용까지
백신 기반 접근도 후반부 임상 단계에 도달했다. 스웨덴 제약사 다이아미드메디컬(Diamyd Medical)의 ‘다이아미드(Diamyd, 성분 GAD65 백신)’은 항원 특이 면역피망 바카라 방식으로 개발 중이며, 현재 임상3상(DIAGNODE-3)이 진행되고 있다. 해당 임상은 HLA-DR3-DQ2 유전자형을 보유한 환자군을 대상으로 하며, 톱라인(Top-line) 결과는 오는 2026년 3월 공개될 예정이다.
한편 세포 이식과 유전자 전달 기술을 융합한 차세대 피망 바카라제 개발도 속도를 내고 있다. 미국 셀트랜스(CellTrans)의 ‘란티드라(Lantidra, 성분 도니슬레셀·Donislecel)’는 2023년 FDA 승인을 받아 저혈당 무자각 환자에서 인슐린 독립을 가능하게 한 첫 세포피망 바카라제로 기록됐다.
캐나다 바이오기업인 세르노바(Sernova)는 이식형 장치인 ‘셀 파우치(Cell Pouch)’를 활용해 췌도세포 내성을 최소화하는 전략을 추진하고 있다. 미국 세락시스(Seraxis)는 복막주름(omentum)에 이식하는 클러스터 세포피망 바카라제 후보물질인 ‘SR-02(개발코드명)’의 첫 임상을 진행 중이다.
유전자편집 기반 플랫폼에서도 차세대 피망 바카라제 개발이 활발히 진행 중이다. 미국 사나바이오테크놀로지(Sana Biotechnology)의 ‘SC451(개발코드명)’, 독일 에보텍(Evotec)과 다국적 제약사 노보노디스크(Novo Nordisk, 이하 노보)의 공동 프로젝트인 ‘QR-Beta(개발코드명)’ 그리고 미국 시길론테라퓨틱스(Sigilon Therapeutics, 이하 시길론)의 ‘SIG-002(개발코드명)’ 등이 대표적이다.
다만 에보텍과 노보가 공동으로 개발하던 ‘QR-Beta’ 프로그램은 최근 전략적 검토 끝에 개발이 중단됐다. 또 시길론은 2023년 기존 파트너사인 다국적 제약사 일라이릴리(Eli Lilly. 이하 릴리)에 인수되면서 세포피망 바카라 자산이 릴리의 포트폴리오에 통합돼, 유전자 편집과 세포피망 바카라 융합 분야에서의 상업화 전략이 강화됐다.
미국 코어파마슈티컬스(COUR Pharmaceuticals, 이하 코어)와 다국적 제약사 오츠카(Otsuka Pharmaceutical)는 면역관용 유도 피망 바카라제 후보물질인 ‘OFP-310(또는 개발코드명 CNP-103)’을 개발하고 있다. 이 후보물질은 GAD65 항원특이 나노입자 기술을 기반으로 하며, T세포 면역관용 유도를 통해 제1형 당뇨병의 자가면역반응을 억제하는 것을 목표로 한다. 오츠카는 아시아 지역 상업화 권리를 보유하고 있으며, 코어와의 협력을 통해 임상 개발을 병행 중이다.
또 미국 아이톨러런스(iTolerance)는 ‘iTOL-101(개발코드명)’과 ‘iTOL-102(개발코드명)’ 두 후보물질을 전임상 단계에서 연구하고 있다. 두 후보 모두 ‘조절 T세포(Treg)’ 활성화 펩타이드와 줄기세포 융합 플랫폼을 기반으로 개발 중이며, 이식 내성 유도와 세포 생착 효율 개선을 목표로 한다.

