- 퓨쳐켐, PET 60% vs PCWG3 14%…정정 공시로 논란 촉발
- 노바티스 ‘플루빅토’, RECIST ORR 29.80%
- 셀비온, RECIST ORR 35.90%…PCWG3 ORR 41.03%
- 직접 비교 어려워…PFS·OS 지표가 궁극적 판단 기준 전망
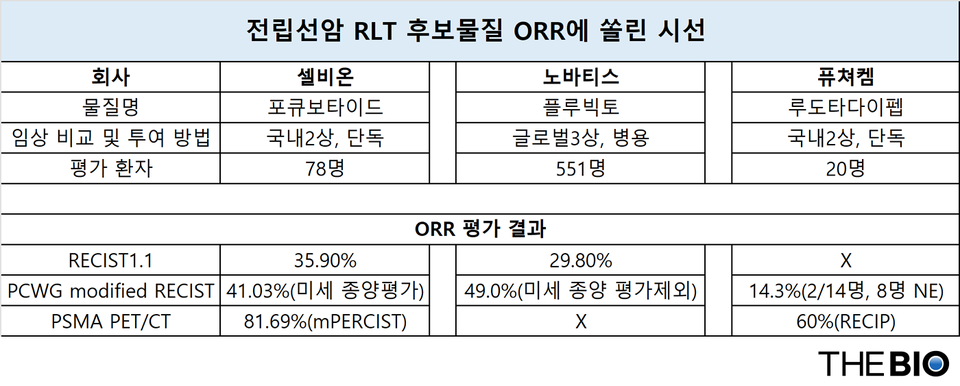
[더바이오 지용준 기자] 거세 저항성 전립선암(mCRPC) 방사성리간드치료제(RLT)의 객관적 반응률(ORR) 평가 방식에 업계의 관심이 쏠리고 있다. 국내 RLT 개발기업들은 다국적 제약사 노바티스의 ‘플루빅토’에 이어 계열 내 최고(Best-in-class) 약물 개발에 도전하고 있다. 이들은 유의미한 ORR 개선을 내세우고 있지만, 평가 기준에 따라 결과는 다소 엇갈리고 있다.
17일 업계에 따르면, 퓨쳐켐은 최근 한국거래소의 보완 요청에 따라 ‘루도타다이펩(개발코드명 FC705)’의 임상2상 최종결과보고서(CSR) 결과를 정정 공시했다. 이는 지난 4월 해당 결과가 최초로 공시된 지 5개월 만에 이뤄졌다. 이번 정정 공시에서 2차 지표 중 하나였던 ‘PCWG3 modified RECIST v1.1 기준 ORR’은 14.3%(2/14명)에 그쳤다. 5개월 전 퓨쳐켐이 발표한 ‘PSMA PET/CT 안전한 바카라 사이트 방식의 ORR’ 60%와 비교해 격차가 컸다.
퓨쳐켐은 “대상자 중 골전이만 있는 환자가 많아 전체의 57.1%(8/14명)이 평가 불가(NE, Not Evaluable)로 분류됐다”며 “연조직 병변이 없는 뼈 병변은 PCWG-modified RECIST로 평가할 수 없기 때문에 모수가 줄어든 결과이며, 통계학적으로 의미가 없다는 취지에서 최초 공시에서 제외했다”고 설명했다.
이번 퓨쳐켐의 ORR 수치 변경은 그동안 플루빅토 대비 ‘우월성’을 강조해왔던 만큼 논란을 야기했다. 모호한 ORR 기준 때문이다. 실제 퓨쳐켐은 다른 안전한 바카라 사이트 방식으로 이뤄진 노바티스의 ORR과 직접 비교하며 우월성을 강조하기도 했다.
고형암 임상에서 ORR 반응을 안전한 바카라 사이트하는 국제적인 기준은 ‘CT/MRI를 통한 RECIST v1.1 방법’이다. 전립선암의 경우에는 ‘PCWG-modified RECIST v1.1’이 최근 안전한 바카라 사이트 방법으로 활용되고 있다. PCWG-modified RECIST v1.1은 골전이 반응을 Bone Scan과 CT·MRI 판독 결과를 결합해 전반적인 치료 반응을 안전한 바카라 사이트할 수 있도록 한 기준이다.
‘PSMA PET/CT’는 전립선암 환자의 림프절·골전이를 탐지하는데 높은 민감도를 보인다. 다만 의료기관별 기기 보유 격차로 접근성에 한계가 있고, 양성 병변 정의에서도 이질성이 존재한다는 지적이 나온다.
노바티스는 플루빅토의 임상3상(VISION)에서 ORR 안전한 바카라 사이트 ‘RECIST v1.1’를 활용했으며, 추가 분석에서는 ‘PCWG-modified RECIST v1.1’을 적용한 평가 결과도 함께 제시했다. 반면 PSMA PET/CT는 임상 평가지표로 활용하지 않았다.
국내 RLT 개발기업인 셀비온 역시 자사의 RLT 후보물질인 ‘포큐보타이드’의 임상2상에서 RECIST v1.1과 PCWG-modified RECIST 두 기준을 병행해 ORR을 제시했다. PSMA PET/CT는 보조적 지표로 활용했다.
ORR은 안전한 바카라 사이트 방식에 따라 차이를 보였다. 특히 같은 임상 데이터라 하더라도 기준 적용 방법에 따라 편차가 커지는 경향을 띠었다.
노바티스의 플루빅토는 임상3상 RECIST v1.1 안전한 바카라 사이트서 ORR이 29.8%, PCWG-modified RECIST v1.1에서는 ORR이 49.0%를 보였다. 단 플루빅토의 PCWG-modified RECIST v1.1 평가는 림프절 ≥15㎜와 연조직 병변 ≥10㎜ 이상 등 CT/MRI로 반복 측정 가능한 병변을 기준이 제시되면서 골전이에 나타날 수 있는 작은 병변들은 제외된 ORR 결과다.
셀비온의 경우 mCRPC RLT 후보물질인 포큐보타이드 1차 유효성 평가지표인 RECIST v1.1 기준에 따른 ORR은 35.90%, PCWG modified RECIST v1.1 안전한 바카라 사이트선 41.03%로 집계됐다. 셀비온은 “PCWG modified RECIST v1.1 평가 결과에 대해 경화성 골전이 병소의 변화를 세밀하게 평가해 전립선암의 특성을 반영했다”고 밝혔다. PSMA PET/CT는 ‘mPERCIST’ 방식으로 ORR이 81.69%로 집계됐다. mPERCIST는 병변의 섭취 강도 변화를 평가하는 방식이다.
퓨쳐켐은 루도타다이펩의 임상2상에서 RECIST v1.1 기준으로 ORR 안전한 바카라 사이트를 진행하지 않았다. PSMA PET/CT ‘RECIP 1.0’ 안전한 바카라 사이트 방식으로 ORR 60%가 산출됐다. RECIP 1.0은 PSMA 발현 병변의 부피 변화를 안전한 바카라 사이트하는 방법이다. 반면 PCWG modified RECIST v1.1에서는 뼈 전이 환자가 안전한 바카라 사이트 결과에서 제외되며 14.3%의 ORR을 기록했다.
업계에서는 ORR에서 주요 수치가 확인된 만큼, 향후 영상학적 무진행 생존기간(rPFS)과 전체 생존기간(OS) 등이 치료제 효과를 가를 핵심 지표가 될 것이라는 분석이 나온다. 셀비온과 퓨쳐켐 양사 모두국내 ‘조건부 허가’를 신청하겠다는 입장을 밝힌 상태다.
셀비온은 포큐보타이드가 노바티스의 플루빅토 대비 아시아인 대상 통계적 우월성을 확보함으로써 베스트 인 클래스 가능성을 입증했다고 밝혔다. 퓨쳐켐은 루도타다이펩이 임상3상에 진입한 만큼, PSMA PET/CT 기반 조건부 허가를 타진하고 있다.

